Алюминий и сталь гальваническая пара
Совместимость металлов или как избежать гальванической коррозии?

Контактная коррозия происходит при непосредственном контакте двух разнородных металлов. Нельзя, к примеру, соединять алюминиевые листы медной заклепкой, так как при определенных условиях они образуют сильную гальваническую пару.
Разные металлы имеют разные электродные потенциалы. В присутствии электролита один из них играет роль катода, а другой анода. В результате химической реакции, протекающей между ними, начнется коррозионный процесс, в котором медь (катод) будет беспощадно разрушать алюминий (анод).
Почти все пары разнородных металлов, находящиеся в контакте между собой, подвержены коррозии, так как даже влага из воздуха может выступить в роли электролита и активировать их электродный потенциал. Но одни пары уязвимы в большей степени, а другие – в меньшей.
Например, алюминий отлично контактирует с оцинкованной сталью, хромом и цинком, а латунь совершенно не «дружит» со сталью, алюминием и цинком. Чтобы узнать, какие металлы совместимы, а какие нет, обратимся к основам химии.
В ряду электрохимической активности металлы стоят в следующей последовательности:

Электрохимический ряд напряжения металлов
Для примера рассмотрим пару алюминий – медь. Алюминий стоит в ряду слева от водорода и имеет электроотрицательный потенциал равный -1.7В, а медь находится справа и имеет положительный потенциал +0.4В. Большая разница потенциалов приводит к разрушению более активного алюминия. Медь сильнее всех, впереди стоящих элементов, поэтому в паре с любым из них она выйдет победителем. Чем дальше друг от друга в ряду стоят элементы, тем выше их несовместимость и вероятность протекания гальванической коррозии.
Данные о совместимости некоторых металлов представлены в таблице:
| Алюминий | Латунь | Бронза | Медь | Оцинкованная сталь | Железо | Свинец | Нержавеющая сталь | Цинк | |
| Алюминий | Д | Н | Н | Н | Д | О | О | Д | Д |
| Медь | Н | О | О | Д | О | Н | О | Н | Н |
| Оцинкованная сталь | Д | О | О | О | Д | О | Д | О | Д |
| Свинец | О | О | О | О | Д | Д | Д | О | Д |
| Нержавеющая сталь | Д | Н | Н | Н | О | О | О | Д | Н |
| Цинк | Д | Н | Н | Н | Д | Н | Д | Н | Д |
Д – абсолютно допустимые контакты (низкий риск ГК);
О – ограничено допустимые контакты (средний риск ГК);
Н – недопустимые контакты (высокий риск ГК).
Приведенная таблица может служить кратким справочником для определения совместимости некоторых конструкционных металлов. Допустимость и недопустимость контактов разнородных в электрохимическом отношении металлов устанавливает ГОСТ 9.005-72.
Пример недопустимых гальванических пар:

Гальваническое действие может возникнуть, если строительную конструкцию из нержавеющей стали скреплять оцинкованными болтами. В этой нежелательной паре пострадает высоко анодный крепеж, поскольку его электроны будут перемещаться в направлении катодной нержавеющей стали. Поэтому, крепежные детали должны быть изготовлены из менее гальванически активного металла, чем материал металлоконструкции.

На скорость течения гальванокоррозии оказывает влияние площадь поверхности анода и катода. Если большой по размеру анод соединить с маленьким катодом, то анод будет ржаветь медленно, а если сделать наоборот, то быстро. Например, используйте болты из нержавеющей стали для крепления алюминия, но не наоборот.
Степень интенсивности протекания контактной коррозии зависит и от условий эксплуатации соединения. В обычных атмосферных условиях процесс будет протекать менее быстро и возрастает в агрессивной электропроводной среде, например, растворах кислот и щелочей. Присутствие в воде других веществ увеличивает проводимость электролита и скорость коррозии. Поэтому при проектировании конструкций важна оценка окружающей среды.
Как защитить конструкцию или узел от контактной коррозии?
Если по конструктивным соображениям невозможно избежать нежелательного контакта разнородных металлов, то можно попытаться уменьшить гальваническую коррозию с помощью следующих методов:
- окраска поверхностей в районе их стыка;
- нанесение совместимых металлических покрытий;
- изоляция соединения от внешней среды;
- электрическая изоляция;
- установка неметаллических прокладок, вставок, шайб в болтовых соединениях.
Практика показывает, что в тех случаях, когда пренебрегают требованиями к допустимости контактов разных металлов, приходится дорого за это расплачиваться. Неправильная компоновка контактных пар выводит из строя узлы крепления, металлоконструкции и может стоять человеческой жизни.
Очень нужная статья. Только бы побольше вариантов крепления с алюминием в трущейся паре
Болты из алюминия — свежо!
Нержавеющая сталь — это в основном железо. Оно рядом с цинком. Кто там пару создаёт?
В целом очень поверхностная заметка.
Очень полезно! Особенно примеры популярных соединений!
Материалы, которые нельзя сочетать при гальванизации
Если железо, методом горячего погружения, покрыть цинком , то получим так называемую гальванизированную сталь. Вступив в химическую связь с металлом, цинк образует антикоррозийное покрытие. Между чистым цинком, образующим верхний слой покрытия, и самим железом, прослаивается оксид цинка. Содержание оксида цинка в процентном соотношении плавно переходит от цинка к железу.
Гальваническая коррозия возникает в тех случаях, когда разные металлы соприкасаются друг с другом в присутствии электролита. Так, например, морская вода, проникающая на лодке повсюду, является отличным электролитом. Рассмотрим электрические потенциалы металлов, которые чаще всего применяются в малом судостроении, с помощью гальванической шкалы, представленной ниже.
Однако не будем углубляться в дебри химии, а для понятия практического смысла, рассмотрим основные детали:
- Из двух металлов, контактирующих между собой, тот, что находится слева, будет подвергаться коррозии.
- В зависимости от следующего условия, безопасной считается разница потенциалов в 0,1 Вольт, а разница в 0,2 Вольта считается приемлемой.
- В зависимости от открытой площади поверхности металлов, коррозия распространяется различными темпами. Лучше, если крепеж изготовлен из более благородного металла, чем само изделие, в таком случае срок его службы будет дольше. В противном случае, он очень скоро начнет подвергаться коррозии.

Если использовать алюминиевые крепежи, то вполне вероятно возникновение проблем, лучше всего использовать монелиевые заклепки, сплав которого состоит из никеля с содержанием меди, железа и марганца.
Используя данные приведенной ниже таблицы, можно самостоятельно решить, для крепления каких деталей, крепежи из какого металла лучше всего использовать. Так, например, детали из нержавеющей стали и алюминия не стоит крепить заклепками из цинка, а крепежи из латуни недопустимы для крепления изделий из бронзы.
| Крепёж | ||
| Материал детали | Допустимо | Недопустимо |
| Оцинкованная сталь | Оцинкованная или нержавеющая | Латунь и бронза |
| Алюминий | Нержавеющая | Оцинкованный, латунь |
| Латунь | Латунь или бронза | Нержавеющая |
| Бронза | Бронза или нержавеющая | Латунь |
| Нержавеющая сталь | Нержавеющая или монель | Оцинкованная или латунь |
Присутствуют сплавы, являющиеся гальваническими парами сами по себе. Примером гальванической пары может служить латунь, соприкасаясь с электролитом, одна из фаз у неё начинает корродировать. Такое свойство называется децинкификацией. Предмет из латуни, который подвергся такому взаимодействию, теряет прочность и очень неприятно выглядит.
Сталь и оцинковка
На борту лодки не стоит иметь предметы из низкоуглеродистой стали, не имеющей защитного покрытия, так как она склонна к коррозии. Если такие изделия покрыты защитным материалом, то их присутствие в лодке вполне допустимо. Достичь этого получается обычно путем нанесения слоя цинка, при этом получается 2 плюса. Цинк отлично справляется с коррозией, а в случае, если присутствует электролит, цинк подвергается коррозии раньше стали.
Известно несколько способов нанесения цинкового слоя, принципиальная разница между которыми заключается в величине толщины формируемого слоя. Для получения срока службы, приемлемого в морской среде, толщина защитного слоя должна быть около 100 мкм. Такой результат, до 125мкм, при горячем погружении, достигается лужением, результат до 40мкм достигается при окраске. Электрогальваника в таком случае не используется, с помощью нее можно достичь покрытия толщиной лишь 20 мкм.
Таким образом, блестящие оцинкованные крепежи, продаваемые в хозяйственных магазинах, могут пригодится лишь при строительстве теплицы, но никак не на лодке, где срок службы его окажется недолговечной. «Морской» крепеж просто обязан быть луженым.
Медь
При строительстве конструкций из дерева, традиционно применяют гвозди, изготовленные из медного материала с шайбами. Такие гвозди являются идеальным материалом для крепления достаточно гибких сооружений. Они устойчивы к коррозии, легко крепятся и являются достаточно гибкими для обеспечения подвижки элементов. Такие корабельные гвозди из меди до сих пор встречаются в продаже, несмотря на появление конструкций из клееных материалов и стеклопластика. Однако замечено снижение выбора таких гвоздей, так, например, пяти-шестимиллиметровые шайбы в продаже уже не найти, в связи с чем строители каноэ вынуждены заниматься расклепкой гвоздей. Исчезают с прилавков и гвозди нестандартных размеров, так необходимые при ремонте обшивки.
Латунь
Латунь традиционно применяется в роли шурупов. Вспоминая о присутствии такой проблемы, как децинкификация, крепежи из латунного материала рекомендуется применять только в защищенных местах, например, внутренняя обстройка или местах, в которых наша жизнь от него не зависит.
Бронза
Кремниевая бронза является стандартным материалом для изготовления крепежей. Используется она при изготовлении гвоздей, болтов, а также шурупов гигантских размеров. Бронза достаточно устойчива к подвержению коррозии и обладает длительным сроком службы (от 30 до 50 лет). Благодаря чему, независимо от дороговизны, крепеж из бронзы достаточно конкурентоспособен.
| Виды медных сплавов и химический состав | ||||
| Наименование | Обозначение | Состав | Применение | |
| Латуни | Обычная латунь | CZ108 | Zn 37% | Внутреннее оборудование |
| Морская латунь | CZ112 | Zn 37%; Sn 1% | Оборудование довоенных лодок | |
| Высокопрочная латунь | CZ114 | Zn 37%; Mn 2%; Al,5%; Fe 1%; Pb 1,5%; Sn 0,8%. | Такелажные скобы, гребные винты, лебёдки | |
| Коррозионностойкая латунь | CZ132 | Zn 36%; Pb 2,8%; As 0,1% | Водозапорная и трубная арматура | |
| Бронзы | Алюминивая бронза | CA104 | Al 10%; Ni 5%; Fe 5% | Высокопрочное оборудование |
| Фосфористая бронза | PB102 | Sn 5%; P 0,2% | Сборное и кованное оборудование | |
| Кремнистая бронза | CS101 | Si 3%; Mn 1% | Крепёж | |
| Оружейная бронза | LG2 | Sn 5%; Pb 5%; Zn 5% | Литьё | |
| Алюминевая бронза для литья | AB2 | Al 10%; Ni 5%; Fe 3% | Леерное и мачтовое оборудование | |
| Al — алюминий, As — мышьяк, Fe — железо, Mn — марганец, Ni — никель, P — фосфор, Pb — свинец, Si — кремний, Sn — олово, Zn — цинк. | ||||
Нежелательно и даже недопустимо создание гальванических пар из алюминия и алюминиевых сплавов в сочетании: с медью и медными сплавами, палладием, серебром, никелем, золотом, хромом, платиной, оловом и родием.
Сплавы из цинка не сочетаются:
- с серебром,
- палладием,
- родием,
- золотом,
- медью и медными сплавами,
- платиной.
Недопустимо сочетание хрома и никеля со следующими металлами:
- медь и медные сплавы,
- палладий,
- родий,
- золото,
- серебро
- и платина.
Нелегированная сталь кадмий, олово и свинец не сочетают:
- с серебром,
- родием,
- платиной,
- палладием,
- золотом.
Сплавы из магния и алюминия не допустимы:
- с золотом,
- хромом,
- серебром,
- свинцом,
- платиной,
- палладием,
- медью,
- родием
- и с легированной и нелегированной сталью.
Свяжитесь с нами любым удобным способом, для получения консультации на любой вид услуги по гальваническому покрытию.
Тел: +7 (960) 850-40-16
Email: info@miriso.ru
Часы работы: Пн-Пт с 9 00 до 18 00
Наши специалисты помогут вам с выбором вида и метода гальванического покрытия.
Форум ребризер-дайверов
| Текущее время: 20 июл 2021, 17:02 |
Часовой пояс: UTC + 3 часа
Коррозия в гальванических парах
Одна из лучших статей о электрохимических реакциях с нержавеющией сталью
и о коррозии нержавейки была опубликована в 2004 году в журнале КАТЕРА И
ЯХТЫ по материалам фирмы Quicksilver Marine Parts & Accessories.
Приведем здесь частично текст и изображения из этой статьи.
Этому виду коррозии подвержены многие металлы, а в особенности —
нержавеющая сталь. «Щель» в данном случае — это пространство под
всевозможными отложениями (песка, ила и т.д.), под пластиковыми шайбами,
фетровыми прокладками и т.д. — иначе говоря, место, из которого попавшая
туда влага не может найти выхода и где образовалась застойная зона.
Нержавеющая сталь — это сплав на основе чугуна, в который входят хром и
никель. Не ржавеет она благодаря образующейся на поверхности изделия
тонкой пленке оксида хрома. При отсутствии кислорода оксидный слой
разрушается, и нержавеющая сталь покрывается ржавчиной не хуже обычной.
Иными словами, «нержавейка» не ржавеет только до тех пор, пока имеется
доступ кислорода . Самый простой способ предотвратить данную
разновидность коррозии — ограничить доступ влаги в «щели», вовремя
удалять образующиеся отложения и обеспечить хорошую вентиляцию
«сомнительных» мест.
ВИДЫ МОРСКОЙ КОРРОЗИИ
Расположенные под водой металлические детали обычно подвергаются двум
типам коррозии: гальванической и так называемой «коррозии от блуждающих
токов».
Гальваническая коррозия представляет собой электрохимическую реакцию
между двумя и более различными (или разнородными) металлами. Различными,
потому что для того, чтобы началась реакция, один должен быть более
химически активным (или менее стабильным), чем другой или другие. Когда
мы говорим про гальваническую коррозию, то имеем в виду электрообмен.
Все металлы обладают электрическим потенциалом, поскольку у всех атомов
есть электроны, движение которых и есть электричество.
Гальваническая коррозия более активного металла начинается в тот
момент, когда две или более детали из разнородных металлов, имеющие
взаимный контакт (благодаря обычному соприкосновению, или же посредством
проводника) помещаются в электролит (любую жидкость, проводящую
электричество). Электролитом может быть что угодно, за исключением
химически чистой воды. Не только соленая морская, но и обычная вода
из-под крана благодаря наличию минеральных веществ является превосходным
электролитом, и с ростом температуры электропроводность ее только растет
(по этой причине корпуса судов, эксплуатирующихся в жарком климате,
заметно больше подвержены коррозии, чем на Севере).
Процесс гальванической коррозии можно наиболее наглядно
проиллюстрировать на примере алюминиевой подводной части подвесного
мотора и гребного винта из нержавеющей стали. Алюминий — более химически
активный металл — является в данном случае анодом, а менее активная
нержавеющая сталь — катодом.
Вот что происходит, когда эта пара помещается в воду, играющую роль
электролита (рис. 1):
1. На аноде:
a. Через место контакта (в нашем случае — через гребной вал) электроны
перетекают с анода, металла более химически активного на катод — гребной
винт. Происходит следующая реакция: Al -> Al+++ +3e.
b. При этом атомы более химически активного металла превращаются в ионы
(этим термином обозначаются атомы с «недостатком» или «избытком»
электронов), которые устремляются в воду и связываются с ионами
кислорода, обмениваясь с ними электронами и образуя оксид алюминия.
(Процесс этот ничем не отличается от того, что происходит с ионами
железа при образовании оксида железа).
c. Образовавшиеся молекулы оксида алюминия либо уносятся потоком воды,
либо оседают на алюминиевой поверхности. Таким образом, подводная часть
вашего подвесника в результате гальванической коррозии буквально
растворяется в воде.
2. На катоде:
a. С анода поступают электроны, причем они не просто накапливаются, а
вступают в реакцию с ионами электролита.
b. Реакция обычно происходит такая:
1 1/2 О2 + 3 Н2О + 6 е -> 6 ОН—.
c. Ион гидроокиси ОН— — щелочной, поэтому в районе катода образуется
щелочная среда. (Следует отметить, что это обстоятельство надо
обязательно иметь в виду владельцам деревянных корпусов — щелочь
разрушает целлюлозу).
Очень важно понять, что следствием освобождения каждого позитивного
иона металла на аноде обязательно является формирование негативного иона
электролита, образующегося вследствие реакции электронов катода.
Электрически анодные и катодные реакции должны быть эквивалентны. Рост
или снижение уровня катодной реакции вызывает ответные рост или снижение
уровня анодной реакции. Это ключевой факт для понимания процесса
коррозии и управления им. Его можно проиллюстрировать эффектом влияния
размеров анода и катода. Если к очень большому аноду подключить
маленький катод, процесс коррозии анода пойдет медленно. А если
поступить наоборот, то анод очень быстро разрушится.
Алюминиевых деталей на катере или мотолодке полным-полно. И если не
контролировать процесс гальванической коррозии, все они быстро выйдут из
строя.
Гальваническая коррозия может протекать даже в том случае, если на
вашей лодке нет ни одной детали из нержавеющей стали. Предположим, что и
подводная часть мотора, и винт алюминиевые, но лодку вы обычно ставите у
пирса со стальной стенкой и подключаетесь при этом к береговой системе
электроснабжения. Провод заземления (так называемый «третий» — дань
безопасности) соединяет при этом алюминиевые детали лодки с погруженной
в воду стальной стенкой (рис. 2). Если учесть внушительную массу
стальной стенки, то и подводной части мотора, и винту грозят серьезные
повреждения. Предотвратить их можно при помощи гальванического изолятора
— своеобразного фильтра, отсекающего токи низкого напряжения и
позволяющего при этом заземляющему проводу в случае пробоя изоляции или
короткого замыкания выполнить свою функцию — отвести ток в землю и
спасти вам жизнь.
НА ЧТО ОБРАЩАТЬ ВНИМАНИЕ
Первый признак гальванической коррозии — вздутие краски на
поверхностях, расположенных ниже ватерлинии, начинающееся обычно на
острых гранях, и образование на обнажившемся металле белесого
порошкообразного налета. Потом на поверхности металла начинают
образовываться заметные углубления — словно кто-то выгрызает из него
кусочек за кусочком.
Гальваническую коррозию подводных частей подвесных моторов и угловых
колонок — или любых алюминиевых частей лодки — значительно ускоряет
наличие деталей из нержавеющей стали, таких, как гребные винты,
триммеры (особенно если они «заземлены» на двигатель), узлы
дистанционного управления. Именно на них и уходят электроны алюминиевых
деталей.
Другая причина, способная ускорить процесс гальванической коррозии —
это уменьшение полезной площади анодных протекторов (о них тоже будет
рассказано позже). Но и без наличия нержавеющей стали расположенные под
водой алюминиевые детали все равно подвергаются воздействию
гальванической коррозии — хотя и не столь интенсивной, как при контакте
с иным металлом. При наличии электролита на большинстве однородных,
вроде бы, металлических поверхностей все равно образуются крошечные
аноды и катоды — в тех местах, где состав сплава неоднороден или имеются
посторонние вкрапления или примеси — например, частицы металла с форм
или штампов.
Нержавеющую сталь в качестве катода и алюминий в качестве анода мы
использовали лишь в качестве одного из примеров; образовать «батарею»
для запуска гальванической коррозии в паре с алюминием способен любой
другой металл. К примеру, такая пара образуется и при контакте алюминия
с цинком, только на сей раз катодом становится алюминий, а подвергается
коррозии цинк — металл более химически активный. Один из худших врагов
алюминия при образовании гальванической пары — это медь или медные
сплавы (бронза).
Резюмируя сказанное рекомендуется всегда обращать внимание при монтаже
на эту простую таблицу активности металлов. Чем дальше друг от друга
стоят металлы в этом ряду, тем больше вероятность возникновения между
ними электрохимической коррозии
Например категорически не рекомендуется использовать нержавеющий крепеж
в контакте с алюминием, особенно если этот узел может быть подвергнут
влиянию влаги.
Еще один пример на основе этой таблицы — соединение электрических
алюминиевых и медных проводов между собой. Для соединения всегда
рекомендуется использовать переходные клеммные колодки, которые есть в
продаже в любом электротехническом магазине.
Другая причина гальванической коррозии — подключение к береговой
электросети. При этом алюминиевая подводная часть вашего мотора или
колонки посредством заземляющего вывода подключается к подводным частям
других лодок и становится частью огромной гальванической батареи,
связанной с погруженным в воду береговым металлом. При этом не только на
вашей лодке, но и на соседних коррозия значительно ускоряется.
КОРРОЗИЯ ОТ БЛУЖДАЮЩИХ ТОКОВ
Произойти подобное может в том случае, если металл, по которому течет
электрический ток, поместить в любой заземленный водоем (в реку, озеро,
море, океан — без разницы, не в счет разве что стеклянный аквариум). Ток
через воду устремится в землю. Следствием этого явится интенсивная
коррозия в том месте, где произошел «пробой». В наихудшем случае та же
алюминиевая подводная часть мотора может разрушиться буквально за
несколько дней.
Данная разновидность коррозии отличается от гальванической, хотя природа
у них одна. Гальваническая коррозия вызывается соединением двух
разнородных металлов и происходит за счет их электрических потенциалов.
Один металл выступает в роли анода, другой — в роли катода. Здесь же
электрический ток попадает на подводную часть лодки из внешнего
источника и через воду уходит в землю.
К примеру, ваша лодка расположена между лодкой с утечкой постоянного
тока и местом, являющимся хорошим заземлением для этого тока. Хотя ток
могут уходить в землю и через воду, ваша лодка может явиться проводником
со значительно меньшим сопротивлением. Таким образом, ток будет уходить
в землю и с нее. Наиболее интенсивно коррозия будет развиваться в том
месте лодки, откуда ток уходит в воду.
Блуждающие токи могут вызываться не только внешними, но и внутренними
источниками — коротким замыканием в сети лодки, плохой изоляцией
проводки, подмокшим контактом или неправильным подключением какого-либо
элемента электрооборудования.
Наиболее распространенный внешний источник блуждающих токов — береговая
сеть электроснабжения. Лодка с внутренним источником блуждающих токов
(например, по причине повреждения изоляции одного из проводов) может
стать причиной усиленной коррозии множества соседних лодок, подключенных
к той же береговой электросети, если они обеспечивают лучшее заземление.
Ток при этом передается на другие лодки посредством все того же
«третьего» заземляющего провода.
Гораздо более неуловимый — но потенциально более опасный — случай
коррозии блуждающих токов может происходить безо всяких проблем с
электрооборудованием (и вашей лодки, и соседних). Предположим, что вы
возвращаетесь на стоянку после выходных на воде, подсоединяетесь к
береговому источнику, чтобы подзарядить аккумулятор, и спокойно уходите
домой — автоматическое зарядное устройство само отключит зарядившуюся
батарею. В понедельник по соседству с вашей лодкой причаливает большой
стальной катер (с ободранной и поцарапанной краской). Владелец его тоже
подключается к береговой сети и тоже оставляет свою посудину на
несколько дней. Электрическая батарея готова — большой стальной корпус
и небольшая подводная часть вашего мотора, соединенные заземляющим
проводом. В зависимости от разделяющего их расстояния, разницы размеров
и времени, которое ваш сосед решил провести на берегу, в следующие
выходные вы можете обнаружить, что подводная часть вашего мотора либо
просто покрыта белесым налетом, либо разрушилась чуть ли не полностью.
Алюминий и сталь гальваническая пара
20 Ноября 2016
Согласно знаменитой поговорке, «электротехника — наука о контактах».
Любому электромонтажнику известно, что нельзя скручивать между собой медный и алюминиевый провода. Медная шина заземления или латунная стойка для платы плохо сочетаются с оцинкованными винтиками, купленными в ближайшем строительном супермаркете — коррозия может уничтожить электрический контакт. Голая алюминиевая деталь вообще может постепенно превратиться в прах, если к ней приложить даже низковольтное напряжение.
В советских ГОСТах было написано почти всё о допустимых контактах металлов, однако сейчас может быть весьма неудобно искать в старых документах информацию о соединениях. Хабраюзер @teleghost собрал все данные в одной таблице.
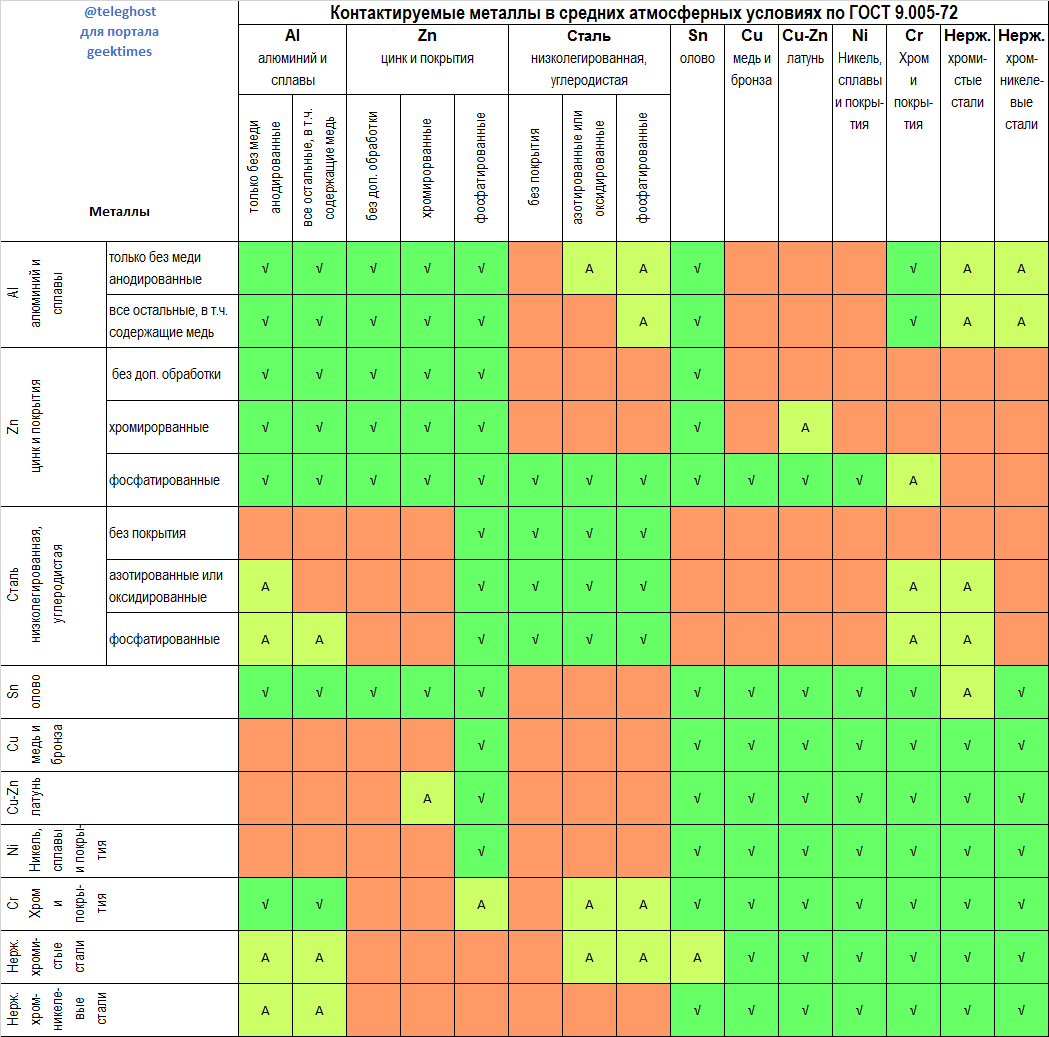
Далее приведена выдержка из ГОСТ 9.005-72 для средних атмосферных (т.е. комнатных) условий. Кликабельно.

Несколько слов о металлах.
Оцинкованная сталь — основная рабочая лошадка народного хозяйства. В виде различных метизов «оцинковка» встречается в магазинах стройматериалов гораздо чаще, чем, например, нержавейка. Фабричные корпуса ПК, технологические ящички и шкафчики для оборудования чаще всего выполнены из оцинкованной холоднокатанной стали толщиной порядка 1мм.
Нержавеющая сталь — королева сталей: прочная, пластичная, стойкая к коррозии, электропроводная, круто выглядит. Слишком тугая, чтобы резать и гнуть её дома в промышленных масштабах. Хромистые и хромисто-никелевые нержавейки электрически плохо совместимы с цинком и «голой» сталью, зато дают надёжный контакт с медью без помощи олова. Алюминий, а также азотированная, оксидированная и фосфатированная низколегированная сталь ограниченно совместимы при стандартных атмосферных условиях. Нержавейка марки А2 не «магнитится», но существуют и нержавеющие стали с магнитными свойствами. Магнитные свойства не влияют на коррозионную стойкость нержавеющей стали.
Алюминий и его сплавы бывают анодированные (с защитным слоем) и обычные (неанодированные). Алюминий легко обрабатывать в домашних условиях, но необходимо помнить о коррозии. Не используйте голый алюминий в качестве проводника даже с низковольтным напряжением, иначе ток медленно обратит деталь в прах. Обработанным в мастерской алюминиевым и дюралюминиевым деталям показана полная эквипотенциальность (наведённые полями токи вроде бы по фиг, заземлять тоже можно). Алюминий совместим с цинковым покрытием, но для контакта с медью, «голой» или никелированной сталью требуется оловянная «прокладка». Ограниченно допустим контакт алюминия с нержавейкой в атмосферных условиях. Для простоты можно принять, что при контакте с другими металлами и покрытиями алюминий будет корродировать сам по себе, без помощи внешнего электричества.
Медь мягкая и довольно неаппетитно окисляется на воздухе, поэтому изделия из меди заключают в герметичную оболочку или лакируют. Латунные бляхи солдатских ремней и стойки для электронных печатных плат лучше сопротивляются окислению и выглядят аппетитнее позеленевшей меди, особенно если их периодически полировать (я про бляхи, конечно). При этом ни медь, ни её сплав с цинком (латунь) «не дружат» с чистым цинком и его покрытиями. Зато медь совмещается с хромом, никелем и нержавейкой. А если вы держите в руках какую-нибудь клемму, то она наверняка из лужёной (покрытой оловом) меди.
Олово относительно стойко к коррозии (в комнатных условиях) и электрически совместимое почти со всем, кроме чугуна, низколегированных и углеродистых сталей и магния. Не стоит паять оловом и бериллий, будьте внимательны при сборке домашнего ядерного реактора. Олово используют, чтобы из недопустимого электрического контакта получить допустимый, т.е. в качестве «прокладки». Клеммы из лужёной меди — отличный пример.
Не следует использовать олово при низких температурах — с прошлого века известна т.н. «оловянная чума» — полиморфное превращение т. н. «белого олова» в «серое» (b-Sn → a-Sn), при котором металл рассыпается в серый порошок. Причина разрушения состоит в резком увеличении удельного объёма металла (плотность b-Sn больше, чем a-Sn). Переход облегчается при контакте олова с частицами a-Sn и распространяется подобно «болезни». Наибольшую скорость распространения оловянная чума имеет при температуре —33°С; свинец и многие др. примеси её задерживают. В результате разрушения «чумой» паянных оловом сосудов с жидким топливом в 1912 погибла экспедиция Р. Скотта к Южному полюсу.

Оловянная чума (распад олова при низких температурах).
Никелем покрыты блестящие «компьютерные» винтики. Такое покрытие совместимо с медью и бронзой, латунью, оловом, хромом и нержавеющей сталью. Никель несовместим с цинком и алюминием (для алюминия лучше контакт с нержавеющей сталью, см. ниже).
Особенности коррозионной агрессивности неметаллов. Приложение 3б к ГОСТ 9.005-72:
- Коррозионная агрессивность органических материалов определяется активностью выделяющихся продуктов старения.
- Коррозионная агрессивность фенопластов, аминопластов, пенопластов, формальдегидных клеев определяется выделением формальдегида, возможностью его окисления до муравьиной кислоты и уротропина, который может быть источником аммиака.
- Коррозионная агрессивность материалов из древесины определяется выделением растворов уксусной и муравьиной кислот.
- Коррозионная агрессивность эпоксидных материалов определяется наличием в них свободного хлора и хлористого водорода, карбоновых и дикарбоновых кислот.
- Коррозионная агрессивность резинотехнических изделий определяется содержанием в них серы и ее соединений, соединений водорода с галогенидами, органических соединений с окислительными свойствами.
- Полимерные материалы, получаемые реакцией конденсации (эпоксидные, полиэфирные и т.п.), обладают наибольшей коррозионной агрессивностью в период отверждения. Процесс отверждения в замкнутых объемах конструкции проводить не рекомендуется.
- Облучение неметалла ионизирующим облучением (ультрафиолетовым, гамма-облучением и т.д.) может увеличивать его коррозионную агрессивность.
- Коррозионная агрессивность неметалла при прямом контакте с металлом определяется его водо- и кислородопроницаемостью. Значения водо- и кислородопроницаемости для ряда неметаллов приведены в табл.4 и 5.
Допустимые и недопустимые контакты металлов. Популярные метрические и дюймовые резьбы
 Электронику часто называют наукой о контактах. Многие знают, что нельзя скручивать между собой медный и алюминиевый провода. Медная шина заземления или латунная стойка для платы плохо сочетаются с оцинкованными винтиками, купленными в ближайшем строительном супермаркете. Почему? Коррозия может уничтожить электрический контакт, и прибор перестанет работать. Если это защитное заземление корпуса, то прибор продолжит работу, но будет небезопасен. Голая алюминиевая деталь вообще может постепенно превратиться в прах, если к ней приложить даже низковольтное напряжение.
Электронику часто называют наукой о контактах. Многие знают, что нельзя скручивать между собой медный и алюминиевый провода. Медная шина заземления или латунная стойка для платы плохо сочетаются с оцинкованными винтиками, купленными в ближайшем строительном супермаркете. Почему? Коррозия может уничтожить электрический контакт, и прибор перестанет работать. Если это защитное заземление корпуса, то прибор продолжит работу, но будет небезопасен. Голая алюминиевая деталь вообще может постепенно превратиться в прах, если к ней приложить даже низковольтное напряжение.
Доступные нам металлы не ограничиваются только медью и алюминием, существуют различные стали, олово, цинк, никель, хром, а также их сплавы. И далеко не все они сочетаются между собой даже в комнатных условиях, не говоря уже о жёстких атмосферных или морской воде.
В советских ГОСТах было написано почти всё о допустимых контактах металлов, но если изучение чёрно-белых таблиц из 1000 ячеек мелким шрифтом утомляет, то правильный ответ на «медный» вопрос — нержавейка, либо никелированная сталь, из которой, кстати, и сделан почти весь «компьютерный» крепёж. В эпоху чёрно-белого телевидения были другие понятия об удобстве интерфейса, поэтому для уважаемых читателей (и для себя заодно) автор приготовил цветную шпаргалку.
И, раз уж зашла речь о металлообработке, заодно автор привёл таблицу с популярными в электронике резьбами и соответствующими свёрлами, отобрав из объёмных источников наиболее релевантное по тематике портала. Не все же здесь слесари и металлурги, экономьте своё время.
Преамбула
Да, в век 3D-печати популярность напильника с лобзиком несколько потускнела. Но клетка Фарадея для РЭА по-прежнему является преимуществом, не забываем и про защитное заземление. Да, для печати корпусов РЭА уже доступен электропроводный (conductive) ABS-пластик, но судя по источнику, его удельное сопротивление примерно в миллион раз больше меди. Дескать, пыль уже не липнет, но для заземления всё равно многовато. Напечатать же стальные детали корпуса ПК в домашних условиях пока никак невозможно, да мы и алюминий-то с оловом никак не освоим…
Что же делать? Нашему брату приходится действовать методом Микеланджело, используя для творчества вместо каменной глыбы купленные в DIY-магазине заготовки, либо вообще старые корпуса ПК. Работая как-то с корпусом от старого сервера IBM из шикарной миллиметровой стали, автор впал в ступор, потому что имеющаяся резьба была крупнее М3, но мельче #6-32 (позже выяснилось, что это М3,5). Зачем вообще понадобилось в 2003-м году использовать метизы М3,5, останется загадкой, но о существовании дробной метрической резьбы автор даже не подозревал.
UPD
Для моддеров, кстати, рынок предлагает новые, удобные инструменты арсенала домашней мастерской, и про один из них (осциллорез) я рассказываю в отдельной публикации. Арсенал принадлежностей прекрасно дополнит более привычные циркулярные мини-пилы (aka «дремели»), а отсутствие эффекта «запрессовки зубьев» упростит обработку вязких металлов типа меди и алюминия. Инструмент лёгкий, не такой неуклюжий и опасный, как «болгарка». Можно пилить металл практически на уровне носа и без риска получить рубящий удар от заклинившего или осколок от «взорвавшегося» диска. А так бывает в красочно описанных уважаемыми читателями случаях с УШМ: 300-граммовый блин «болгарки» делает 200 оборотов в секунду, потребляя до 2кВт электричества, и требует чуть ли не костюм сапёра. Работающий же осциллорез травматологи упирают себе пильной стороной прямо в ладонь, чтобы успокоить пришедшего на снятие гипсовой повязки пациента… Впрочем, вернёмся к нашим металлам.
Допустимые и недопустимые контакты металлов по ГОСТ 9.005-72
DISCLAIMER: Предоставляется «как есть». Если уважаемый читатель занимается моделизмом, автомобилизмом или робототехникой, в ГОСТе также приведены: Таблица №2 для жестких и очень жестких атмосферных условий, Таблица №3 для контактов, находящихся в морской воде. Ниже я предлагаю выдержку из Таблицы №1 для средних атмосферных (т.е. комнатных) условий. Буква «А» означает «ограниченно допустимый в атмосферных условиях», подробности в самом ГОСТе.
Кликабельно (спасибо, НЛО):
Пара слов о металлах
Металлурги, поправляйте, если что не так. Коррозия очень объёмная и сложная тема, и я не претендую на полноту её освещения. Я лишь даю выборочные зарисовки, чтобы сформировать у читателя нужные ассоциативные ряды.
Алюминий и его сплавы бывают анодированные (с защитным слоем) и обычные (неанодированные). Алюминий легко обрабатывать в домашних условиях, но помните о коррозии. Не используйте голый алюминий в качестве проводника даже с низковольтным напряжением, иначе ток медленно обратит деталь в прах. Обработанным в мастерской алюминиевым и дюралюминиевым деталям показана полная эквипотенциальность (наведённые полями токи вроде бы по фиг, заземлять тоже можно). Алюминий совместим с цинковым покрытием, но для контакта с медью, «голой» или никелированной сталью требуется оловянная «прокладка». Ограниченно допустим контакт алюминия с нержавейкой в атмосферных условиях. Для простоты можно принять, что при контакте с другими металлами и покрытиями алюминий будет корродировать сам по себе, без помощи внешнего электричества.
Витая пара из омедненного алюминия (Copper Clad/Coated Aluminium, CCA) — это отдельная история, в домашних условиях кабель всё равно не производится.
Пара слов про case modding
Если вы занимались сборкой ПК, то наверняка знаете, что болтики для монтажа приводов CD/DVD, «ноутбучных» дисков 2.5″ и флоппи-дисководов (ха-ха) используют метрическую резьбу M3. В корпусах ПК и жёстких дисках 3.5″ используется более грубая дюймовая резьба #6-32 UNC. Почему? Мягкий металл любит более грубую резьбу, к тому же адепты дюймовой системы пока лидируют на рынке технологий. Стойка 19″ использует (вы не поверите) дюймы в качестве основной меры, однако для монтажа оборудования я встречал только оцинкованные клетевые шайбы и винты с метрической резьбой М6. Дюймово-метрический дуализм в технологиях…
Обустройство своей инженерной кухни я начал с того, что купил защитные очки, набор качественных свёрл по металлу, небольшой вороток и метчики на резьбы M3 и #6-32 UNC, а заодно M4 и M6. Плашки не понадобились.
Популярые виды резьбы, используемой в компьютерной технике
ГОСТ 19257-73 рекомендует использовать следующие диаметры свёрл для металлов. Наверное, стоит учитывать и количество метчиков в наборе: чем твёрже материал, тем больше необходимость в «предварительных» метчиках. У меня их по три штуки, два «грубых» и один «финишный». А как правильно, кстати?
UPD
А как правильно — читайте комментарии, на публикацию-таки зашли мастера слесарного дела, только я не успел отсортировать всю информацию. Пользователь golf2109 любезно принёс сюда прямо из мастерской два правых столбца таблицы для обозначения того, как мягкость (вязкость) металла влияет на диаметр отверстия под резьбу, благодарю за поддержку.
| Диаметр резьбы | Стандартный шаг, мм | Диаметр сверла, мм | ||
| ГОСТ | Fe | Al | ||
| M2 | 0.4 | 1,6 | 1.5* (-0.1) | |
| M2,5 | 0.45 | 2.0 | 1.8* (-0.2) | |
| M3 | 0.5 | 2.5 | 2.3 (-0.2) | |
| M3.5 | 0.6 | 2.9 | 2.7* (-0.2) | |
| M4 | 0.7 | 3.3 | 3.2 | 3.0 (-0.3) |
| M5 | 0.8 | 4.2 | 3.9 (-0.3) | |
| M6 | 1.0 | 5.0 | 4.9 | 4.6 (-0.4) |
| M8 | 1.25 | 6.8 | 6.7 | 6.3 (-0.5) |
| M10 | 1.5 | 8.5 | 8.0 (-0.5) | |
| #6-32 UNC | 0.794 | 2.85 | 2.7* | 2.5* (-0.35) |
* Я рискнул прикинуть калибры двух дополнительных свёрл для стали и алюминия там, где по ним у меня нет данных в источниках. Обратите внимание, резьба #6-32 UNC по наружному диаметру находится между M3 и M4, а по шагу резьбы вообще ближе к M5.
UPD
Если сверлите что-то толще миллиметрового листа, читайте спойлер про СОЖ .
 На известной китайской площадке можно приобрести «пальцевые» винтики (thumb screw), причём и на #6-32, и на M3. Материал и цвет разный.
На известной китайской площадке можно приобрести «пальцевые» винтики (thumb screw), причём и на #6-32, и на M3. Материал и цвет разный.
Источники
» ГОСТ 9.005-72. Единая система защиты от коррозии и старения. Машины, приборы и другие технические изделия. Допустимые и недопустимые контакты металлов. Общие требования.
» ГОСТ 19257-73. Отверстия под нарезание метрической резьбы. Диаметры.
» Unified Coarse Thread ANSI B1.1 (резьбы UNC ANSI B1.1).
ⓘ Энциклопедия | Гальваническая пара — Вики ..
Отрывок, характеризующий Гальваническая пара
– Ayez confiance en Sa misericorde, [Доверьтесь Его милосердию,] – сказала она ему, указав ему диванчик, чтобы сесть подождать ее, сама неслышно направилась к двери, на которую все смотрели, и вслед за чуть слышным звуком этой двери скрылась за нею. Пьер, решившись во всем повиноваться своей руководительнице, направился к диванчику, который она ему указала. Как только Анна Михайловна скрылась, он заметил, что взгляды всех, бывших в комнате, больше чем с любопытством и с участием устремились на него. Он заметил, что все перешептывались, указывая на него глазами, как будто со страхом и даже с подобострастием. Ему оказывали уважение, какого прежде никогда не оказывали: неизвестная ему дама, которая говорила с духовными лицами, встала с своего места и предложила ему сесть, адъютант поднял уроненную Пьером перчатку и подал ему; доктора почтительно замолкли, когда он проходил мимо их, и посторонились, чтобы дать ему место. Пьер хотел сначала сесть на другое место, чтобы не стеснять даму, хотел сам поднять перчатку и обойти докторов, которые вовсе и не стояли на дороге; но он вдруг почувствовал, что это было бы неприлично, он почувствовал, что он в нынешнюю ночь есть лицо, которое обязано совершить какой то страшный и ожидаемый всеми обряд, и что поэтому он должен был принимать от всех услуги. Он принял молча перчатку от адъютанта, сел на место дамы, положив свои большие руки на симметрично выставленные колени, в наивной позе египетской статуи, и решил про себя, что всё это так именно должно быть и что ему в нынешний вечер, для того чтобы не потеряться и не наделать глупостей, не следует действовать по своим соображениям, а надобно предоставить себя вполне на волю тех, которые руководили им. Не прошло и двух минут, как князь Василий, в своем кафтане с тремя звездами, величественно, высоко неся голову, вошел в комнату. Он казался похудевшим с утра; глаза его были больше обыкновенного, когда он оглянул комнату и увидал Пьера. Он подошел к нему, взял руку (чего он прежде никогда не делал) и потянул ее книзу, как будто он хотел испытать, крепко ли она держится. – Courage, courage, mon ami. Il a demande a vous voir. C’est bien… [Не унывать, не унывать, мой друг. Он пожелал вас видеть. Это хорошо…] – и он хотел итти. Но Пьер почел нужным спросить: – Как здоровье… Он замялся, не зная, прилично ли назвать умирающего графом; назвать же отцом ему было совестно. – Il a eu encore un coup, il y a une demi heure. Еще был удар. Courage, mon аmi… [Полчаса назад у него был еще удар. Не унывать, мой друг…] Пьер был в таком состоянии неясности мысли, что при слове «удар» ему представился удар какого нибудь тела. Он, недоумевая, посмотрел на князя Василия и уже потом сообразил, что ударом называется болезнь. Князь Василий на ходу сказал несколько слов Лоррену и прошел в дверь на цыпочках. Он не умел ходить на цыпочках и неловко подпрыгивал всем телом. Вслед за ним прошла старшая княжна, потом прошли духовные лица и причетники, люди (прислуга) тоже прошли в дверь. За этою дверью послышалось передвиженье, и наконец, всё с тем же бледным, но твердым в исполнении долга лицом, выбежала Анна Михайловна и, дотронувшись до руки Пьера, сказала: – La bonte divine est inepuisable. C’est la ceremonie de l’extreme onction qui va commencer. Venez. [Милосердие Божие неисчерпаемо. Соборование сейчас начнется. Пойдемте.] Пьер прошел в дверь, ступая по мягкому ковру, и заметил, что и адъютант, и незнакомая дама, и еще кто то из прислуги – все прошли за ним, как будто теперь уж не надо было спрашивать разрешения входить в эту комнату.
Совместимость металлов или как избежать гальванической коррозии?
Контактная коррозия происходит при непосредственном контакте двух разнородных металлов. Нельзя, к примеру, соединять алюминиевые листы медной заклепкой, так как при определенных условиях они образуют сильную гальваническую пару.
Разные металлы имеют разные электродные потенциалы. В присутствии электролита один из них играет роль катода, а другой анода. В результате химической реакции, протекающей между ними, начнется коррозионный процесс, в котором медь (катод) будет беспощадно разрушать алюминий (анод).
Почти все пары разнородных металлов, находящиеся в контакте между собой, подвержены коррозии, так как даже влага из воздуха может выступить в роли электролита и активировать их электродный потенциал. Но одни пары уязвимы в большей степени, а другие – в меньшей.
Например, алюминий отлично контактирует с оцинкованной сталью, хромом и цинком, а латунь совершенно не «дружит» со сталью, алюминием и цинком. Чтобы узнать, какие металлы совместимы, а какие нет, обратимся к основам химии.
В ряду электрохимической активности металлы стоят в следующей последовательности:
Для примера рассмотрим пару алюминий – медь. Алюминий стоит в ряду слева от водорода и имеет электроотрицательный потенциал равный -1.7В, а медь находится справа и имеет положительный потенциал +0.4В.
Большая разница потенциалов приводит к разрушению более активного алюминия. Медь сильнее всех, впереди стоящих элементов, поэтому в паре с любым из них она выйдет победителем.
Чем дальше друг от друга в ряду стоят элементы, тем выше их несовместимость и вероятность протекания гальванической коррозии.
Данные о совместимости некоторых металлов представлены в таблице:
| Алюминий | Латунь | Бронза | Медь | Оцинкованная сталь | Железо | Свинец | Нержавеющая сталь | Цинк | |
| Алюминий | Д | Н | Н | Н | Д | О | О | Д | Д |
| Медь | Н | О | О | Д | О | Н | О | Н | Н |
| Оцинкованная сталь | Д | О | О | О | Д | О | Д | О | Д |
| Свинец | О | О | О | О | Д | Д | Д | О | Д |
| Нержавеющая сталь | Д | Н | Н | Н | О | О | О | Д | Н |
| Цинк | Д | Н | Н | Н | Д | Н | Д | Н | Д |
– абсолютно допустимые контакты (низкий риск ГК);
О
– ограничено допустимые контакты (средний риск ГК);
Н
– недопустимые контакты (высокий риск ГК).
Приведенная таблица может служить кратким справочником для определения совместимости некоторых конструкционных металлов. Допустимость и недопустимость контактов разнородных в электрохимическом отношении металлов устанавливает ГОСТ 9.005-72.
Пример недопустимых гальванических пар:
Гальваническое действие может возникнуть, если строительную конструкцию из нержавеющей стали скреплять оцинкованными болтами.
В этой нежелательной паре пострадает высоко анодный крепеж, поскольку его электроны будут перемещаться в направлении катодной нержавеющей стали.
Поэтому, крепежные детали должны быть изготовлены из менее гальванически активного металла, чем материал металлоконструкции.
На скорость течения гальванокоррозии оказывает влияние площадь поверхности анода и катода. Если большой по размеру анод соединить с маленьким катодом, то анод будет ржаветь медленно, а если сделать наоборот, то быстро. Например, используйте болты из нержавеющей стали для крепления алюминия, но не наоборот.
Степень интенсивности протекания контактной коррозии зависит и от условий эксплуатации соединения.
В обычных атмосферных условиях процесс будет протекать менее быстро и возрастает в агрессивной электропроводной среде, например, растворах кислот и щелочей.
Присутствие в воде других веществ увеличивает проводимость электролита и скорость коррозии. Поэтому при проектировании конструкций важна оценка окружающей среды.
Как защитить конструкцию или узел от контактной коррозии?
Если по конструктивным соображениям невозможно избежать нежелательного контакта разнородных металлов, то можно попытаться уменьшить гальваническую коррозию с помощью следующих методов:
- окраска поверхностей в районе их стыка;
- нанесение совместимых металлических покрытий;
- изоляция соединения от внешней среды;
- электрическая изоляция;
- установка неметаллических прокладок, вставок, шайб в болтовых соединениях.
Практика показывает, что в тех случаях, когда пренебрегают требованиями к допустимости контактов разных металлов, приходится дорого за это расплачиваться. Неправильная компоновка контактных пар выводит из строя узлы крепления, металлоконструкции и может стоять человеческой жизни.


