Где взять никель в домашних условиях?
Никелевый лом

Широкое распространение в качестве легирующей добавки получил металл никель, прием лома которого производится как для чистового вещества, так и любых его включений в соединениях и сплавах. Небольшое содержание Ni в различных сталях требует особых условий его приемки, оснащения пунктов специальными приборами спектрального анализа – анализатора металлов.
Для сдачи металла, предпочтительнее выбирать специализированные места приемки, оборудованные под проведение анализа на содержание никеля в ломе, где цена за кг металлических отходов будет выше.
Виды никелевого лома (вторсырья)
Условно, лом отходы никеля можно распределить по физическому состоянию на несколько базовых категорий: кусковой лом, стружка и прочее вторсырье, например, катодные крючки с наросшим слоем этого металла. В зависимости от содержания Ni, каждая из них разбивается на несколько подгрупп:
- Лом из чистого металла;
- Шлаковые отходы. Характеризуются содержанием Ni до 85 %;

- Сдаваемые на металлолом сплавы, где никель один из основных компонентов. Это широко известный нихром, в котором концентрация Ni составляет 55 – 78%, а также малознакомые большинству пермаллой (до 76 %), константан, нейзильбер и прочие;
- Вторичные сплавы, легированные никелем. Лом нержавейки и отходы этого вида, как правило, различные марки сталей с небольшим его содержанием. Долевая концентрация элемента Ni в жаропрочных и нержавеющих материалах доходит до 20%, тогда как у низколегированных сталей эта величина не превышает 5 %;
- Никельсодержащий шлам, представляющий гальванические и металлургические виды отходов.

Все перечисленное вторсырье, активно скупается пунктами приемки. Стандартно, цена за кг лома никеля определяется процентным содержанием последнего в металлических отходах.

Также к лому никеля будут относиться:
- никелевые катализаторы;
- закись никеля (NiOH);
- гидрат закиси никеля (Ni(OH)2);
- агломераты и концентраты никелевые и т.п.;
- аккумуляторы ТНЖ;
- Отходы, содержащие Ni, как чистый металл.

Существенный сегмент подобных вторичных металлов составляют отработанные никелевые аноды и катоды, которые легко детектируются невооруженным глазом, при наличии определенного опыта. Они обладают светло-серым цветом, отработанные элементы обычно покрыты зеленоватым налетом. При накаливании, никелевые электроды приобретают желтый оттенок, также они характеризуются короткой красной искрой, магнитятся. Поверхность никелевых катодов пупырчатая, тогда как анодов – гладкая.
Следующий распространенный источник поступлений металла на пункты приемки – гранулированный никель, ломом или отходами его назвать сложно, но можно сдать его по высокой цене. Исключение составляют ферроникелевые гранулы. Они, как и гранулированные марки металла H0 – H4, используются для легирования сталей, однако имеют более низкую приемочную стоимость, поскольку это не чистый Ni, а его сплав с железом. Гранулированный ферроникель можно отличить по цвету: металл характеризуется матово-серым оттенком. Напротив, гранулам никеля присущ металлический блеск.

Еще две группы составляют стружка и проволока. Второй компонент, как лом Ni, обнаружить значительно проще. Из никелевой проволоки изготовлены термопары, электроды для гальванопластики, а также сетка, используемая при катализе.

Обмотка струн из никеля
Цены на лом никеля
Мы собрали цены по всей России и вычислили средние. Поэтому Вы смело можете ориентироваться на указанную ниже стоимость за 1 килограмм никелевого лома.
Цены на нихром и никель-содержащие сплавы
Цены на никель
Сплавы на базе элемента Ni
Данный вид вторичного цветного металла хоть и уступает в цене за кг лому никеля, остается довольно прибыльным товаром на рынке сдачи металлолома. Достаточно эффективно принимаются сплавы никеля с металлами:
- хром;
- медь;
- железо.
Жаростойкий нихром – соединение на базе Ni (60 – 80%) и Сr. Марка сплава Х15Н60 дополнительно включает железо. Данный материал на вторичный рынок поступает в виде нагревательных элементов, после эксплуатации внутри устройств теплового воздействия: обжиговые печи, сушки и прочее. Также нихром можно встретить среди деталей, эксплуатируемых при высоких температурах: реостаты, подложки для систем напыления.

Проволока марки Х15Н60
Сплавы меди и никеля представлены достаточно широким спектром соединений (в скобках указано содержание Ni):
- Монель (29 – 70%). Используется никельсодержащий сплав как конструкционный материал в авиационном и судовом машиностроении. Многие узлы оборудования для нефтяной и химической промышленности: бурильные инструменты, насосные валы, скребки, лезвия и прочее; также изготовлены из монели. Цена лома зависит от никелевого содержания, которое устанавливается по наименованию марки или анализатором. Не следует путать со сплавом МНЦ, в отличие от него, монель не содержит цинка;
- Пермаллой (45 – 82%). В состав соединения также входит железо и хром. Источники лома этого сплава: трансформаторы, экранирующие оболочки катушек, реле. Высокое содержание железа в соединении приводит к тому, что отходы пермаллоя часто сдаются как вторичный чермет. Приемка сплава как никельсодержащий лом производится специализированными ломозаготовительными предприятиями, оборудованными спектральными анализаторами. Оплата производится, исходя из присутствия элемента Ni;

Корпуса кожухов для трансформаторов, выполненные из пермаллоя
- Константан (39 – 41%). Из этого соединения изготовлены термопары, реостаты, а также электронагревательные элементы, эксплуатируемые при рабочих температурах до 500 °C. Встречается константан в измерительных приборах низкого класса точности;

- Мельхиор (5 – 30%). Этот никельсодержащий сплав находится на слуху, благодаря посуде и монетам СССР номиналом 10, 15 и 20 копеек (находились в обращении до денежной реформы 61-го года). Менее известно соединение, как материл для изготовления термогенераторов, резисторов высокой точности, а также деталей субмарин. Мельхиор используется при создании художественных предметов: подсвечники, шкатулки и прочие. Поэтому, определенные изделия из мельхиора, сдавать просто как никельсодержащий лом не всегда выгодно;

Ложка из мельхиора
- Нейзильбер (5 – 35%). Сплав отличается от мельхиора присутствием цинка в составе соединения. Применение нейзильбера также отличается разнообразием направлений. При его участии создается посеребренная посуда, многие художественные предметы. С другой стороны нейзильбер востребован как твердый и упругий сплав при изготовлении булавок, застежек, а также пружин для релейной электротехники. Различные виды медицинских инструментов, паровая и водяная арматура – исполнены из этого соединения.

Проволока нейзильбер – мягкая
Еще один вид сплавов, представляющих интерес как вторичный металл, составляют соединения никеля с железом, например, инвар. Соединение широко используется в точном приборостроении, из него изготавливаются мерные эталоны, деталей часовых механизмов, в частности балансиры хронометров. Дополнительно, этот никельсодержащий сплав – материал для массивных реек геодезической техники, например нивелиров.

Никельсодержащие стали
Еще один источник никеля под лом или отходы представляет собой «нержавейка». Известное свойство этого металла улучшать антикоррозионные свойства нержавеющей стали обеспечивает его широкое использование в различных марках соединения, как с хромом, так и без него. Например, аустенитные, не содержащие хрома стали, отличаются высокой коррозионной стойкостью в агрессивных средах: кипящих щелочах, растворах серной кислоты.
Наиболее популярные, на пунктах приема лома никеля, марки стали:
- Б19, содержание Ni составляет 13 – 15%.
- Б26, требуемая химия для приемки – 9.3%.
- Б28, включает до 19%.
- Б55, диапазон никелевых включений колеблется от 12 до 17%.
Ряд других марок стали, также характеризуются присутствием легирующей добавки элемента Ni, однако с небольшим содержанием этого метала, не превышающим 8%. Впрочем, это не снижает их востребованности, как лома никельсодержащих сплавов.
Резюме
Следует помнить, что вторичный никель может находиться в широком ряде изделий, от промышленных деталей до бытовых и художественных предметов. Это могут быть сломанные медицинские инструменты, бижутерия и даже никелированные кастрюли.
Отдельный раздел лома, отходов никеля можно отвести под аккумуляторы. Даже вытесненные Ni-Cd накопители электрической энергией, были заменены металл гибридными перезаряжаемыми батарейками. Они также содержат никель, который если внимательно осмотреться встречается практически во всех сферах деятельности человека. Необходимо только знать это и найти пункт приема, проводящий оценку отходов на базе специализированных приборов.
Собирая никельсодержащий лом необходимо учитывать, что Ni отнесен к опасным для здоровья человека веществам, в частности может проявляться контактная аллергия на коже.
Секреты никелирования металлических предметов в домашних условиях
Никелирование изделий из металлов позволяет не только защитить их поверхности от коррозии, но и создать на них блестящее покрытие. Такие изделия широко применяются при изготовлении сантехники, автомобильных запчастей, медицинских инструментов и т. д. В связи с этим многие люди задаются вопросом, можно ли выполнить никелирование стали в домашних условиях?
Технология никелирования металлов
Никелирование осуществляется путем нанесения на металлический предмет тонкого слоя никелевого покрытия. Покрыть никелем можно изделия из различных металлов, таких как:
- сталь;
- медь;
- титан;
- алюминий.




Существуют металлы, которые нельзя никелировать:
- олово;
- свинец;
- кадмий;
- сурьма.




Никелевое покрытие обеспечивает защиту изделия от воздействия влаги и различных агрессивных веществ. Часто его наносят в качестве слоя-основы перед хромированием деталей. После нанесения тонкой пленки никеля, напыления из серебра, золота и других металлов держатся более прочно.
В домашних условиях применяются способы, не требующие использования специализированного оборудования. Благодаря этому, никелирование стали, меди, алюминия в бытовых условиях доступно практически каждому человеку. Чтобы получить равномерное покрытие, необходимо предварительно подготовить деталь.

Как подготовить изделие к никелированию?
Подготовка изделия довольно трудоемкий процесс. Следует полностью исключить наличие коррозии, окислений и т. п. Подготовка проводится в несколько этапов.
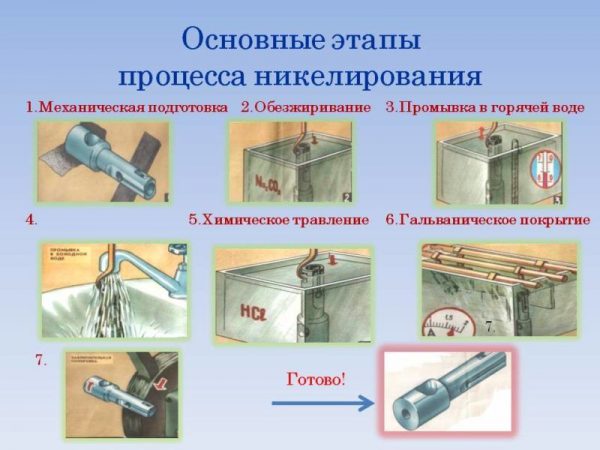
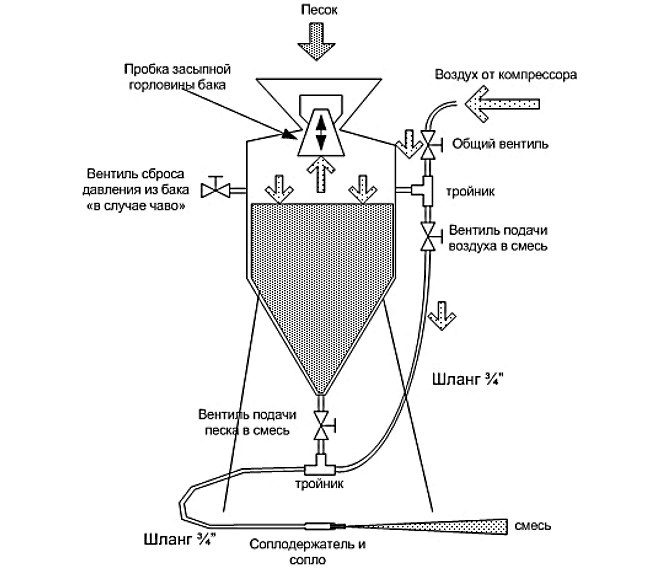
Обработка пескоструйным аппаратом
Данный вид обработки можно выполнять как специализированным пескоструйным аппаратом, так и самодельным. Во время обработки нужно постараться убрать как можно больше посторонних наслоений с поверхности заготовки. Особое внимание следует обратить на труднодоступные места. Они должны быть очищены так же, как и другие участки поверхности.
Шлифовка
Чтобы никелевое покрытие получилось равномерным, нужно максимально выровнять поверхность. Шлифовка дает возможность очистить предмет от оксидной пленки. Для выполнения этого этапа используется наждачная бумага, а также различные инструменты и приспособления, предназначенные для шлифовки.

Совет: не стоит пренебрегать шлифовкой заготовок, неправильная подготовка может привести к отслоению покрытия.

Устранение жировых загрязнений
После того, как процесс шлифовки окончен, следует смыть образовавшиеся загрязнения под проточной водой. Затем потребуется провести обезжиривание заготовки. Для этого можно использовать как готовые, так и самодельные растворители. После нанесения растворителя деталь нужно еще раз промыть водой и тщательно просушить.
Внимание: при выборе растворителя необходимо учитывать степень его воздействия на металл, из которого выполнено изделие. Запрещается применять обезжиривающие растворы, вступающие в химическую реакцию с поверхностью.

Омеднение
Никелирование изделия лучше проводить с предварительным омеднением заготовки. Этот этап не является обязательным, но никелирование стали и других металлов будет более качественным, если покрытие наносится на тонкий слой меди.
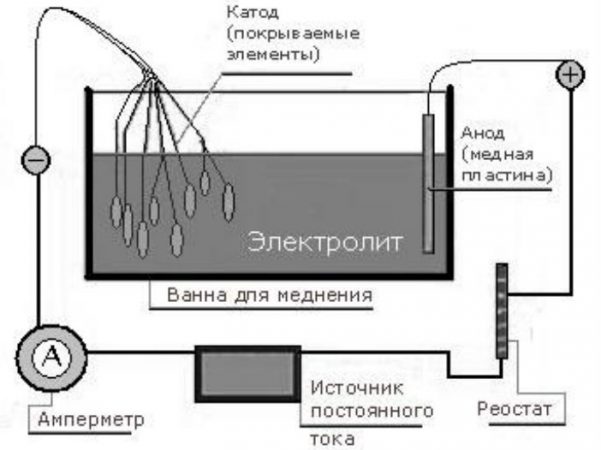
Для омеднения детали необходимо поместить ее в стеклянную емкость с водным электролитом, состоящим из медного купороса и серной кислоты. Предмет подвешивается на проводе таким образом, чтобы он не касался стенок и дна емкости. По обе стороны от заготовки размещаются медные пластины, являющиеся электродами. После этого к электродам и заготовке подключается источник постоянного тока. Степень омеднения прямо зависит от времени проведения процесса.
Способы нанесения никелевого покрытия
Никелирование изделия в домашних условиях можно выполнить двумя способами: химическим и электролитическим.
Электролитический метод
Нанесение покрытия с использованием электролита называется гальваническим никелированием. Сначала потребуется подготовить водный раствор (электролит). Для этого необходимы следующие компоненты:
- сернокислый никель – 70 г;
- сернокислый магний – 15 г;
- поваренная соль – 2.5 г;
- сернокислый натрий – 25 г;
- борная кислота – 10г;
- вода – 500г.






Каждый из компонентов нужно отдельно растворить в воде и профильтровать. Полученные растворы смешивают и заливают в стеклянную емкость. Для гальванического никелирования в сосуд с электролитом помещают никелевые электроды. Чтобы покрытие на заготовке было равномерным, со всех сторон устанавливают не менее двух электродов.
Подготовленную заготовку помещают в сосуд между электродами таким образом, чтобы она не касалась стен и дна емкости. Электроды соединяют между собой медными проводниками, и подключают к плюсовому контакту источника постоянного тока. Токопроводящий провод подключают к минусовому выводу.
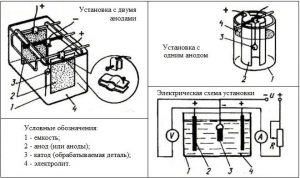
В процессе никелирования стали напряжение питания не должно превышать 6 Вольт. Следует контролировать плотность тока, она не должна превышать 1,2 А. Процесс занимает около 30–40 минут. По его окончании, предмет нужно промыть проточной водой и тщательно просушить. Нанесенное покрытие должно получиться матовым и гладким. Чтобы поверхность изделия приобрела блеск, потребуется выполнить ее полировку.
Химический метод
Никелирование стали и других металлов химическим способом отличается от гальванического прочностью покрытия. При помощи химического никелирования можно легко нанести вещество даже на самые труднодоступные места.
Для выполнения процесса потребуется:
- янтарно-кислый натрий – 7.5 г;
- хлористый никель – 12.5 г;
- гипофосфит натрия – 15 г;
- вода – 500 мл.



В эмалированную посуду наливают воду и растворяют в ней янтарно-кислый натрий и хлористый никель. Затем раствор нагревают до температуры 90 градусов. По достижению требуемой температуры добавляется гипофосфит натрия. Изделие аккуратно подвешивается над емкостью с раствором. Количество жидкости рассчитывается исходя из того, что в 1 литре раствора можно покрыть поверхность площадью 2дм 2 .
Никелирование контролируется визуально: когда деталь равномерно покроется пленкой, процесс завершается. По окончании, деталь нужно промыть в растворе, изготовленном из воды и небольшого количества мела. После этого осуществляют сушку и полировку детали.

Как увеличить срок службы покрытия?
Полученное покрытие имеет пористую структуру. Поэтому металл изделия подвержен коррозии. Чтобы снизить риск ее возникновения, слой никеля покрывают смазочными составами. После их нанесения предмет погружают в емкость с рыбьим жиром. Спустя 24 часа, его излишки убирают при помощи растворителя.
Если изделие имеет крупные габариты, и погрузить его в емкость невозможно, то его поверхность просто натирают рыбьим жиром. Данную процедуру потребуется проводить дважды, с промежутком времени около 12 часов. Через 48 часов после обработки остатки жира нужно удалить.

Выполнить никелирование стали в домашних условиях можно двумя способами. Данный процесс является несложным, но требует тщательной подготовки и предельной аккуратности при выполнении. Необходимо приобрести качественные компоненты для приготовления раствора, заранее подготовить рабочую зону, емкости, инструменты и устройства.
В процессе работы важно соблюдать меры безопасности: защитить глаза и кожные покровы от попадания химических веществ, обеспечить достаточную вентиляцию помещения, предотвратить возможность воспламенения смеси и электрической установки.
Видео по теме: Химическая металлизация — никелирование
Советы по никелированию в домашних условиях
[Никелирование] – это процесс нанесения на металлическую поверхность очень тонкого слоя никеля.
Толщина никелевого слоя, в зависимости от поставленной задачи, размеров детали и дальнейшего ее использования, находится в диапазоне от 0,8 до 55 мкм.
Никелевое черное напыление защищает металлический предмет от разрушительного воздействия внешней среды – окисления, коррозии и реакции с солью, щелочью и кислотой.

Предметами, которым может потребоваться такая защита, являются:
металлические изделия, которые будут находиться на открытом воздухе;
кузовные детали автотехники и мототехники, в том числе и из алюминия;
медицинское и стоматологическое оборудование;
изделия, имеющие длительный контакт с водой;
декоративное металлическое ограждение, в том числе и из алюминия;
предметы, подвергающиеся контакту с сильнодействующими химическими веществами и прочее.
Как можно заметить, технология различного никелирования применяется не только в промышленности, а черное вполне может потребоваться в домашних условиях, своими руками.
Рассмотрим основные методы нанесения защитного слоя своими руками в домашних условиях, металлы, позволяющие наносить никель, тонкости и особенности каждого процесса.
На практике применяются два способа нанесения никелевого слоя — электролитический и химический.
Не будем изучать тонкости промышленного процесса, а опишем проведение в домашних условиях.
Технология нанесения никелевого слоя представлена на видео.
Электролитическое никелирование
Перед электролитическим никелированием (по-другому его еще называют гальваническое ) нужно выполнить электрохимическое меднение детали или заготовки.
Есть два метода, включающие гальваническое — с погружением в раствор электролита и без погружения.
В первом случае, предмет из металла тщательно обрабатывается наждачной бумагой, с него удаляется оксидная пленка, производится промывка сначала в теплой воде для удаления растворителя, а затем в содовом растворе и опять в воде.
В стеклянную емкость поместите два анода из меди и деталь, зафиксировав ее проволокой между пластинами анодов.
Электрохимическое меднение в домашних условиях будем производить с помощью электролита, состоящего из воды с включением 20%-го медного купороса и 2% серной кислоты.
Ток нужно рассчитать из показателей 10-15 мА/кв.см.
Через полчаса обработки током на детали будет тонкий слой меди, а чем дольше будет производиться электрохимическое меднение, тем толще будет слой.
Если деталь большая или отсутствуют подходящие стеклянные емкости, то можно использовать электрохимическое меднение без погружения в электролит.
Для этого делаем кисточку из меди (можно применить многожильный медный провод, конечно, сняв изоляцию только на концах), которую присоединяем к плюсу источника тока и фиксируем с помощью деревянной палочки.
Зачищенную обезжиренную пластинку из металла положим в достаточно широкую стеклянную емкость, зальем раствором электролита (можно взять насыщенный медный купорос) и подсоединим к минусу источника тока.
Теперь макаем кисточку в электролит и проводим возле поверхности детали. Важно постоянное наличие раствора на медной кисточке.
Через некоторое время вы заметите, что на поверхности обрабатываемой детали появился медный слой. Чем толще будет нанесено покрытие из меди, тем меньшее количество пор останется.
Так, например, на 1 кв.см при однослойном нанесении меди будет несколько десятков сквозных пор, а при трехслойном их практически не будет.
Добейтесь нужной толщины меди и можно приступать к следующему этапу.
Нанесение никелевого слоя (гальваническое) производится аналогично процессу меднения с погружением в электролит.
Так, деталь, подвешенная на проводке, и никелевые аноды опускаются в электролит, проволоки от анодов подключаются к плюсу, а проволока от детали – к минусу.
В качестве электролита можно рекомендовать один из двух растворов:
Сернокислые никель, натрий и магний в пропорциях 14:5:3, 0,5% поваренной соли и 2% борной кислоты;
30% сульфата никеля, 4% хлорида никеля и 3% борной кислоты.
Сухие смесь заливаем одним литром нейтральной воды, тщательно перемешиваем и при необходимости избавляется от выпавшего осадка, и применяем как электролит при электролитическом никелировании.
Гальваническое достаточно проводить в течение получасового воздействия постоянного тока с мощностью 5,8-6 В.
В результате обработки током через электролит мы получим матовый неравномерный слой серого цвета. Чтобы выровнять его, предмет из металла необходимо аккуратно зачистить и провести полировку.
Эта технология не может быть применена для деталей с шершавым покрытием или имеющих узкие и глубокие отверстия.
В этом случае нужно использовать химический метод никелирования или чернения деталей.
Технология чернения заключается в том, что на металл наносится промежуточное покрытие из цинка или никеля, а сверху деталь покрывается тонким, не более 2мкм, черное покрытие из никеля.
Декоративное металлическое ограждение, сделанное из деталей с черным никелированием, будет хорошо сохраняться и красиво смотреться.
В некоторых случаях требуется провести никелирование и хромирование.
Метод химического никелирования
Технология химического никелирования деталей заключается в том, что заготовку из металла погружают в кипящий раствор на определенный срок, за который на ее поверхность оседают частички никеля.
Электрохимическое воздействие отсутствует, ток не понадобится.
Технология направлена на получение прочного сцепления никелевого слоя с металлом (особое качество сцепления поверхности и нанесенного слоя наблюдается при никелировании стали и железа).
Химическое никелирование различных деталей реально проводить в условиях гаража или небольшой мастерской.
В эмалированной посуде смешивают сухие реактивы и заливают их водой;
Доводят полученную жидкую смесь до кипения и только тогда доливают гипофосфит натрия;
Погружают в емкость с жидкостью заготовку так, чтобы она не касалась краев и дна. Фактически потребуется установка химического никелирования, которую можно сделать самостоятельно из эмалированного таза соответствующего размера и диэлектрического кронштейна, на который будет подвешиваться заготовка;
В зависимости от применяемого раствора, кипение должно продолжаться от часа до трех;
Заготовку достают и промывают водой, содержащей погашенную известь, после чего можно произвести полировку.
Все составы для химического никелирования деталей будут содержать в обязательно порядке никель хлористый или сернокислый, натрия гипофосфит различной кислотности и какую-то из кислот.
Смеси, содержащие свинец, увеличивают скорость нарастания никелевого слоя до 95 мкм/ч.
Технология предусматривает обработку 20 кв.см поверхности в одном литре раствора.
Кислыми составами производят нанесение никелевого слоя на черные металлы, а щелочные лучше подойдут для нержавеющей стали.
Никелевая пленка, нанесенная на металл без меднения, имеет слабое сцепление с поверхностью. Для его улучшения можно применить термическую обработку, выдержав заготовку при температуре выше 450 градусов;
Нагревать до этой температуры закаленные изделия нельзя, при нагреве до 350-400 градусов они будут терять твердость. Эта проблема решается более длительным выдерживанием, но при температуре в диапазоне 250-300ºС;
При нанесении никелевого слоя на громоздкие детали возникает необходимость перемешивания раствора, что приводит к потребности проводить постоянную фильтрацию. Это основная сложности при проведении процесса не в промышленных условиях.
Аналогичным образом, но с применением другого состава, можно покрыть детали слоем серебра. Серебрение часто применяется для рыболовных снастей с целью предотвратить потускнение крючков и блесен.
Технология нанесения серебра несложная и отличается от никелирования составом электролита, временем и температурой рабочего раствора (для получения ровного слоя серебра требуется состав, подогретый до 90 градусов).
Растворы серебра можно приготовить из воды, ляписа аптечного и 10% солевого раствора.
Выпавший осадок серебра промыть и смешать с 2% гипосульфитом, профильтровать, добавить меловую пыль и размешивая, добиться сметанообразного состояния.
Этой смесью можно натирать металл до образования на нем слоя серебра.
Хранение этого раствора допускается в течение нескольких суток, раствор серебра, допускающий длительное — до полугода хранение, можно приготовить следующим образом: 15 г ляписа, 55 г лимонной кислоты (годится кулинарная) и 30 г хлористого аммония.
Все компоненты растираются в пыль и смешиваются. Порошок для нанесения серебра хранится в сухом виде.
Для работы мокрой салфеткой коснитесь смеси и разотрите ее по обрабатываемой поверхности.
Напыление серебра наносится на очищенную деталь, но готовить ее специальным способом не нужно.
Приведенные способы нанесения никеля и серебра на металлические детали легко повторить самостоятельно в домашних условиях.
Иногда можно столкнуться с необходимостью никелирования алюминия. Никелирование алюминия процесс достаточно дорогостоящий и ненадежный. Электролит для никелирования алюминия стоит достаточно дорого, но частенько идет пузырями.
Проблема в никелировании алюминия в домашних условиях состоит в слабой адгезии — блестящий никель «рвет» покрытие.
Для химического никелирования алюминия подойдет такой состав:
- Никель сернокислый — 20г/л;
- Натрий уксуснокислый — 10г/л;
- Натрий фосфорноватистокислый — 25г/л;
- Тиомочевина, раствор концентрацией 1 г/л — 3мл;
- Фтористый натрий — 0,4г/л;
- Уксусная кислота — 9мл
Никелирование в домашних условиях – получение красивых и надежных покрытий
Покрывая никелем детали из цветных металлов и стали, повышают их сопротивление воздействию коррозионных процессов и механического износа. Никелирование в домашних условиях доступно каждому и характеризуется несложной технологией.
1 Никелирование металлических поверхностей – азы технологии
Никелирование заключается в нанесении на поверхность обрабатываемого изделия тонкого никелевого покрытия, толщина которого, как правило, составляет 1–50 мкм. Этой операции детали подвергают с целью их защиты или для получения характерного (матово-черного или блестящего) внешнего вида никелируемой поверхности. Покрытие, независимо от оттенка, надежно предохраняет металлические предметы от коррозии на открытом воздухе, в растворах солей, щелочей, слабых органических кислот.
Как правило, никелируют детали, изготовленные из стали или таких металлов и сплавов из них, как медь, алюминий, цинк, реже – титан, марганец, молибден, вольфрам. Нельзя обрабатывать химическим никелированием поверхности изделий из свинца, олова, кадмия, висмута, сурьмы. Никелевые покрытия используют в различных промышленных отраслях для защитно-декоративных и специальных целей или в качестве подслоя.

Эту технологию применяют при восстановлении поверхности изношенных деталей различных механизмов и автомобилей, покрытия измерительного и медицинского инструментов, предметов и изделий домашнего обихода, химической аппаратуры, деталей, эксплуатируемых под незначительными нагрузками в условиях воздействия крепких растворов щелочей или сухого трения. Существует 2 метода нанесения покрытий из никеля – электролитический и химический.

Второй несколько дороже, чем первый, однако позволяет получать равномерное по толщине и качеству покрытие на всей поверхности детали, при условии, если обеспечен доступ раствора ко всем ее участкам. Никелирование в домашних условиях является вполне осуществимой задачей. Перед началом работ изделие тщательно очищают от загрязнений и ржавчины (если есть), обрабатывают мелкой наждачной бумагой, чтобы снять оксидную пленку, промывают водой, затем обезжиривают и еще раз промывают.
2 Секреты увеличения стойкости и срока службы никелевых покрытий
Перед никелированием стали желательно выполнять меднение изделия (покрывать подслоем меди). Эта технология используется в промышленности, как отдельный процесс, а также как подготовительный перед серебрением, хромированием, никелированием. Меднение, предваряющее нанесение других слоев, позволяет выровнять дефекты поверхности и обеспечивает надежность и долговечность внешнего защитного покрытия. Медь держится на стали очень прочно, а другие металлы осаждаются на нее гораздо лучше, чем на чистую сталь. Помимо этого, никелевые покрытия не сплошные и на 1 см2 имеют сквозные (до металла подложки) поры:
- несколько десятков – для однослойных покрытий никелем;
- несколько – для трехслойных.

В результате этого коррозионным процессам подвергается металл подложки, находящийся под никелем, при этом возникают условия, провоцирующие отслаивание защитного покрытия. Поэтому, даже при предварительном омеднении, многослойном никелировании, а особенно при однослойном на чистую сталь, необходима обработка поверхности защитного покрытия из никеля специальными составами, которые закрывают поры. При самостоятельной обработке в домашних условиях возможны следующие способы:
- протереть деталь с покрытием кашицеобразной смесью воды с окисью магния и сразу же погрузить ее на 1–2 минуты в 50 % состав соляной кислоты;
- протереть 2–3 раза поверхность детали легко проникающим смазочным составом;
- сразу после обработки еще не остывшее изделие погрузить в рыбий жир (невитаминизированный, лучше старый, который уже непригоден по прямому назначению).

В двух последних случаях излишки смазки (жира) удаляют с поверхности через сутки бензином. В случае обработки больших поверхностей (молдингов, бамперов автомашин) рыбий жир используют следующим образом. В жаркую погоду им протирают деталь 2 раза с промежутком в 12–14 часов, а через 2 суток удаляют излишки бензином.
3 Электролитическое никелирование в домашних условиях
Этот способ требует подготовки электролита, состав которого следующий:
- 140 г сернокислого никеля;
- 50 г сернокислого натрия;
- 30 г сернокислого магния;
- 5 г поваренной соли (хлористого натрия);
- 20 г борной кислоты;
- 1000 г воды.
Химикаты растворяют по отдельности в воде, полученные растворы фильтруют, после чего смешивают. Готовый электролит наливают в емкость. Для гальванического никелирования необходимы электроды из никеля (аноды), которые опускают в ванну с электролитом (одного электрода недостаточно, так как полученное покрытие будет неравномерным). Между анодами на проволочке подвешивают деталь. Медные проводники, идущие от никелевых пластин, соединяют в одну цепь и подключают к положительному выводу источника постоянного тока, провод от детали – к отрицательному.

Для управления силой тока в цепь включают сопротивление (реостат) и миллиамперметр (прибор). Напряжение источника тока должно быть не больше 6 В, плотность тока необходимо поддерживать на уровне 0,8–1,2 А/дм2 (площади поверхности изделия), температура электролита комнатная 18–25 оC. Ток подают 20–30 минут. За это время образуется никелевый слой толщиной примерно 1 мкм. Затем деталь вынимают, как следует промывают водой и просушивают. Полученное покрытие будет серовато-матового цвета. Чтобы слой никеля приобрел блеск, поверхность детали полируют.
Если нет сернокислого натрия и магния, то берут больше сернокислого никеля, доводя его количество в электролите до 250 г, а также борной кислоты – 30 г, натрия хлористого – 25 г. Никелирование в этом случае проводят при значениях плотности тока в пределах 3–5 А/дм2, раствор нагревают до 50–60 оC.

Недостатки электролитического метода:
- на рельефных, неровных поверхностях никель осаждается неравномерно;
- невозможность нанесения покрытия в глубоких и узких полостях, отверстиях и тому подобного.
4 Химическое никелирование изделий в домашних условиях
Все составы для проведения химического никелирования универсальны – пригодны для обработки любых металлов. Готовят растворы, соблюдая определенную последовательность. В воде растворяют все химреактивы (исключая гипофосфит натрия). Посуда должна быть эмалированная. Затем раствор нагревают, доводя его температуру до рабочей, после чего растворяют гипофосфит натрия. Деталь завешивают в жидком составе, температуру которого поддерживают на необходимом уровне. В 1 л подготовленного раствора возможно провести никелирование изделия, площадь поверхности которого до 2 дм2.
Используют следующие составы растворов, г/л:
- Натрий янтарно-кислый – 15, никель хлористый – 25, натрия гипофосфит – 30 (кислотность раствора pH – 5,5). Рабочая температура смеси – 90–92 °С, скорость наращивания покрытия – 18–25 мкм/ч.
- Никель сернокислый – 25, натрий янтарно-кислый – 15, натрия гипофосфит – 30 (pH – 4,5). Температура – 90 °С, скорость – 15–20 мкм/ч.
- Никель хлористый – 30, кислота гликолевая – 39, натрия гипофосфит – 10 (рН – 4,2). 85–89 °С, 15–20 мкм/ч.
- Никель сернокислый – 21, натрий уксуснокислый – 10, свинца сульфид – 20, натрия гипофосфит – 24 (pH – 5). 90 °С, до 90 мкм/ч.
- Никель хлористый – 21, натрий уксуснокислый – 10, натрия гипофосфит – 24 (pH – 5,2). 97 °С, до 60 мкм/ч.
- Никель хлористый – 30, кислота уксусная – 15, свинца сульфид – 10–15, натрия гипофосфит – 15 (pH – 4,5). 85–87 °С, 12–15 мкм/ч.
- Никель хлористый – 30, аммоний хлористый – 30, натрий янтарно-кислый – 100, аммиак (25 % раствор) – 35, натрия гипофосфит – 25 (pH – 8–8,5). 90 °С, 8–12 мкм/ч.
- Никель хлористый – 45, аммоний хлористый – 45, натрий лимоннокислый – 45, натрия гипофосфит – 20 (pH – 8,5). 90°С, 18–20 мкм/ч.
- Никель сернокислый – 30, аммоний сернокислый – 30, натрия гипофосфит – 10 (pH – 8,2–8,5). 85 °С, 15–18 мкм/ч.
- Никель хлористый – 45, аммоний хлористый – 45, натрий уксуснокислый – 45, натрия гипофосфит – 20 (pH – 8–9). 88–90 °С, 18–20 мкм/ч.

По истечении нужного времени изделие промывают в воде, содержащей небольшое количество распущенного мела, затем просушивают и полируют. Полученное таким способом покрытие сталь и железо держат достаточно прочно.
В основе химического процесса никелирования лежит реакция, при которой никель восстанавливается из раствора солей на его основе в присутствии гипофосфита натрия и при помощи остальных химических реактивов. Применяемые составы делят на щелочные (уровень pH превышает 6,5) и кислые (показатель рН составляет 4–6,5). Последние лучше использовать для обработки черных металлов, меди, латуни, а щелочные предназначены для никелирования нержавеющих сталей.

Использование кислых составов позволяет получать на полированном изделии более гладкую, равномерную поверхность, чем с помощью щелочных. У кислых растворов есть и другая немаловажная особенность – вероятность их саморазряда при превышении значений рабочей температуры меньше, чем у щелочных. Никелирование, своими руками выполненное, с использованием щелочных составов гарантирует более прочное и надежное сцепление слоя никеля с металлом, на который произведено его нанесение.
 tutankanara
tutankanara
Живой Журнал
Сергея Подгорных
— В продолжениие темы о юных химиках.
Многие начинающие (и не начинающие) химики задаются вопросом: «А где же взять реактивы?» Оглянитесь! Они вокруг вас! Не верите? Тогда читайте дальше
Итак, начнем. (Это далеко не полный список реактивов, которые можно найти)
ГДЕ ДОСТАТЬ МЕТАЛЛЫ
Алюминиевая пудра — серебрянка. Бывает, продаётся хозмагах(там же где и краски)
Литий Li — встречается в пальчиковых батарейках ENERGIZER Lithium
Натрий Na — в выпускных клапанах двигателей внутреннего сгорания ЗИЛ
Никель Ni — в некоторых батарейках (никелевый стакан)
Свинец Pb — продается в рыболовном магазине как грузило или как пули для пневматичекого оружия (Не шарики!) .
Так же, можно использовать дробь или свинцовые пластины из аккумуляторов (везде содержатся примеси!)
Олово Sn — продается в радиотоварах (припой), но это сплав. Так же, можно поискать и чистое олово( цена его высока) в тех же радиомагах или в химмагах.
Отличительная особенность чистого олова от его сплавов: пруток его хрустит, будучи погнутым
Магний Mg — в магазине под названием магниевые аноды на боллер. Также картеры автомобилей ЗАЗ изготовлены из этого металла, а точнее из сплава электрон.
Серебро Ag — в виде серебряного лома (ложки, кольца и т.п.) Почти во всех случаях — это сплав, для получения чистого серебра необходимо производить очистку
ГДЕ ДОСТАТЬ КИСЛОТЫ
Серная кислота H2SO4 — продается в автомагазинах как кислотный электролит для аккумуляторов (25-30% раствор)
Ортофосфорная кислота H3PO4 — продается как преобразователь ржавчины или флюс для пайки (Читайте состав!)
Уксусная кислота CH3COOH — обычная уксусная эссенция (70%), продается в любом продуктовом магазине
Кремниевая кислота H2SiO3 — легко изготовить самому: к силикату натрия или калия (канц. клей) приливается любая кислота — выпадает осадок нерастворимой в воде кремниевой кислоты
Борная кислота H3BO3 — продается в аптеке
Лимонная кислота (HOOCCH2)2C(OH)COOH — продается в продовольственных магазинах
Соляная кислота HCl — можно достать на рынке, но маловероятно (прекурсор на территории РФ)
ГДЕ ДОСТАТЬ ОСНОВАНИЯ
Гидроксид натрия NaOH продается в смеси с посторонними веществами в отделе бытовой химии как чистящее средство «крот» (Избегать долгого контакта с воздухом, т.к. гидроксид натрия на воздухе превращается в карбонат! Вдобавок набухает и расплывается)
Гидроксид алюминия Al(OH)3 легко получить самому: к раствору сульфата алюминия приливается раствор гидроксида натрия (избегать избытка гидроксида натрия, т.к. гидроксид алюминия амфотерное основание и в избытке щелочи растворяется, образуется тетрагидроксоалюминат натрия(Na[Al(OH)4]). По этой же причине алюминий растворяется в едких щелочах с образованием всё тех же тетрагидроксоалюминатов. )
Гидроксид цинка Zn(OH)2 получается таким же способом, только берется раствор сульфата цинка (гидроксид цинка тоже амфотерное основание)
Гидроксид меди Cu(OH)2 получается таким же способом, только берется раствор сульфата меди
Раствор аммиака в воде NH4OH — (слабое основание) продается в аптеке как нашатырный спирт или в хоз. магазинах 25% раствор(теперь его достаточно сложно найти — остался 10% в стеклянных бутылках)
Керосин — в хозмаге, применяется как растворитель
Мочевина (или карбамид) (NH2)2CO — продаётся в хозмагах в качестве азотного удобрения. В последнее время, многие удобрения встречаются гуматизированными(оч. грязная: небольшое количество целевого вещества, намешанного с землёй)
Уротропин( (CH2)6(NH2)4 или C6H12N4 ) — продаётся загрязнённым в виде сухого горючего( толстые таблетки ) в хозмагах или охотничьих магазинах.
Сера S — в хозмагах как средство для окуривания теплиц, подвалов и т.п. (комковая сера) Загрязнена всевозможными примесями, как коллоидная сера для приготовления суспензии против цветочных клещей — я брал компании Грин Бэлт в пакетиках по 30г — она дороже комковой серы, но значительно чище.
Толуол C6H5CH3 — продается в хоз.магазине как растворитель 646. Необходима перегонка т.к. это многокомпонентный растворитель с содержанием толуола около 50%
Нитрат аммония NH4NO3 — аммиачная селитра.
Нитрат калия KNO3 — калиевая селитра.
Нитрат натрия NaNO3 — натриевая селитра.
Нитрат кальция Ca(NO3)2 — кальциевая селитра.
Нитрат серебра AgNO3 раньше продавался в аптеках под названием ляпис, но сейчас его сняли с производства.
Нитрат свинца Pb(NO3)2 — получается сплавлением аммиачной селитры с окисью свинца( выделяется много газов, окись добавлять постепенно при активном помешивании)
Хлорид натрия NaCl — это обычная поваренная соль, продается в любом продуктовом магазине
Хлорид калия KCl — в хоз. магазине как удобрение, но там очень много примесей(профильтровать будет нелишним).
Хлорид аммония NH4Cl — средство для пайки (флюс) Читайте состав! (в простонародье нашатырь)
Хлорид кальция (CaCl2) — продается в аптеке (раствор в ампулах). Можно получить нагреванием смеси нашатыря с известью
Иодид калия KI — продается в аптеке как средство против йододефицита (Почитайте аннотацию препарата перед тем как купить, потому что может быть другой состав!)
Сульфат калия K2SO4 — продается в хоз. магазине как удобрение (примесей тоже много)
Сульфат меди или медный купорос CuSO4 — продается в хоз. магазинах( синие кристаллы )
Сульфат магния или магнезия (горькая соль) MgSO4 продается в аптеке в качестве слабительного или в хозмагах как удобрение
Сульфат аммония (NH4)2SO4 может продаваться в хоз. магазинах как удобрение, но его просто изготовить и самому: к раствору аммиака (раствор аммиака берется в небольшом избытке) приливается раствор серной кислоты (смесь разогревается). Если емкость где проходила реакция постоит сутки на воздухе, то избыток аммиака улетучится — получается раствор сульфата аммония. Если требуется получить в твердом виде то можно (как я делал) на крышку из под сыра или масла это выливается и сушится где-то 2-3 суток (этот метод более деликатный, чем выпаривание)
Сульфат железа(III) Fe2(SO4)3 в принципе можно получить так же, как указано выше, только берется железный гвоздь/канц. скрепка (при этом емкость пачкается — покрывается желтым налетом) или окислением железного купороса (сульфата железа(II)) перекисью водорода
Сульфат никеля NiSO4 получается так же, как указано выше, только берется никелевая пластинка.
Сульфат цинка ZnSO4 получается так же, как указано выше, только берется цинковая пластинка.
Гидрокарбонат натрия NaHCO3 — обычная пищевая сода
Карбонат кальция CaCO3 — обычный мел (примеси тальк и др.) или мрамор
Ацетат свинца Pb(CH3COO)2 продается в аптеке как свинцовые примочки.
Можно, так же, получить его растворением свинца(или его окиси) в уксусной кислоте( при добавлении перекиси, реакция пойдёт быстрей)
Ацетат натрия CH3COONa получается приливанием уксусной кислоты к карбонату натрия( не важно, к какому). Раствор, почти не пенящийся после приливания очередной порции у.к, подогревают или оставляют на несколько дней в какой-нибудь открытой ёмкости( чтоб излишки уксусной кислоты выветрились ) и, по возможности, упаривают до начала кристаллизации.

 tutankanara
tutankanara
